Alumno: Luis Menacho
Materia:
La materia es todo aquello que nos rodea, todo y todos estamos formados por materia. la materia ocupa un determinado lugar en el espacio. Se caracteriza por tener masa, peso, volumen.

Propiedades Elementales
- Inercia: Es la dificultad o resistencia que opone un sistema físico o un sistema social a posibles cambios. En física se dice que un sistema tiene más inercia cuando resulta más difícil lograr un cambio en el estado físico del mismo.
- Porosidad: Es la propiedad que tienen los cuerpos de dejarse atravesar por aire, agua, calor, sonido y hasta por los microorganismos.

- Indestructibilidad: propiedad por la cual la materia no puede ser destruida, ni tampoco creada, sólo se puede transformar.
extensión: toda materia ocupa un lugar en el espacio.
- Gravedad: La gravedad, denominada también fuerza gravitatoria, fuerza de gravedad, interacción gravitatoria o gravitación, es la fuerza que experimentan entre sí los objetos con masa. Sus efectos son siempre atractivos y su alcance es infinito.

Propiedades particulares:
- Dureza: Es la resistencia de un mineral que presenta al ser rayado. Un mineral posee una dureza mayor que otro, cuando el primero es capaz de rayar al segundo.

En mineralogía la tenacidad es la resistencia que opone un mineral u otro material a ser roto, molido, doblado o desgarrado, siendo una medida de su cohesión. Para describir las distintas clases de tenacidad en los minerales se utilizan diferentes términos.

Es la propiedad de la materia, que junto a la ductilidad presentan los cuerpos a ser labrados por deformación. Se diferencia de aquélla en que mientras la ductilidad se refiere a la obtención de hilos, la maleabilidad permite la obtención de delgadas láminas de material sin que éste se rompa, teniendo en común que no existe ningún método para cuantificarlas.

La ductilidad es la propiedad que presentan algunos metales y aleaciones cuando, bajo la acción de una fuerza, pueden deformarse sin romperse permitiendo obtener alambres o hilos. A los metales que presentan esta propiedad se les denomina dúctiles.

Es la propiedad en la cual un cuerpo logra estirarse mediante una fuerza y tiene la capacidad de volver ha su estado normal.

Propiedad que presenta un cuerpo de tener capacidad para ocupar un volumen mayor. ejemplo: Los gases

La compresibilidad es una propiedad de la materia a la cual se debe que todos los cuerpos disminuyan de volumen al someterlos a una presión o compresión determinada manteniendo constantes otros parámetros.
En física se denomina tensión superficial al fenómeno por el cual la superficie de un líquido tiende a comportarse como si fuera una delgada película elástica. Este efecto permite a algunos insectos, como el zapatero (Hydrometra stagnorum) , desplazarse por la superficie del agua sin hundirse.

La viscosidad es la oposición de un fluido a las deformaciones tangenciales. Un fluido que no tiene viscosidad se llama fluido ideal, en realidad todos los fluidos conocidos presentan algo de viscosidad, siendo el modelo de viscosidad nula una aproximación bastante buena para ciertas aplicaciones

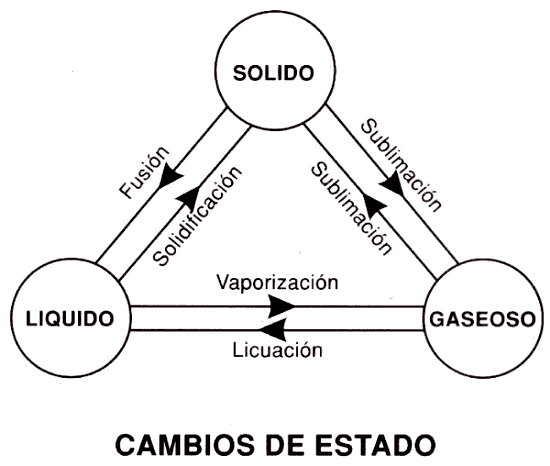
Estados físicos de la materia
Estado físico
Según la agrupación de sus moléculas, los cuerpos tienen cuatro estados diferentes: sólido, líquido, gaseoso y plasma.
Estado sólido
A baja temperatura los cuerpos están en forma sólida tal que los átomos se encuentran unidos formando generalmente estructuras sólidas, en este estado el cuerpo es capaz de soportar golpes sin sufrir una deformación. Presenta las siguientes características:
· Fuerza de cohesión
· Vibración.
· Tiene forma propia.
· No se pueden comprimir.
· Resistentes a fragmentarse.
· Volumen definido.
· Puede ser orgánico o inorgánico.

Estado líquido
Es capaz de fluir y adaptarse a la forma del recipiente que lo contiene. Aún existe alguna ligazón entre los átomos del cuerpo. Presenta las siguientes características:
Fuerza de cohesión menor (regular)
Energía cinética.
Sin forma definida.
Toma el volumen del envase que lo contiene.
En frío se comprime.
Posee fluidez.

Estado gaseoso
Los átomos o moléculas del gas se encuentran libres de modo que son capaces de distribuirse por todo el espacio disponible. Presenta las siguientes características:
Fuerza de cohesión casi nula.
Sin forma definida.
Sin volumen definido.
Se puede comprimir fácilmente.
Ejerce presión sobre las paredes del recipiente que los contiene.

Estado Plasma
Es un sistema que contiene un número significativo de iones libres y cuya dinámica presenta efectos colectivos dominados por las interacciones electromagnéticas de largo alcance entre las mismas.

El estado plasmático todavía lo podemos subdividir en algunos cuantos grupos más:
· Plasma común: las capas de electrones de los átomos son parcialmente deterioradas. Los electrones libres son responsables de las características plasmáticas de la sustancia en cuestión.
· Plasma termonuclear: Las capas electrónicas de los átomos no existen. En éste estado se encuentran el plasma en los núcleos de las estrellas.
· Plasma de nucleones: Debido a muy altas temperaturas o presiones, los mismos núcleos atómicos son despedazados. La materia es una mezcla de electrones, protones y neutrones.
· Plasma de Quarks-gluones: En altas energías los nucleones mismos se desmenuzan en sus constituyentes: los quarks y los gluones.
Ejemplos de plasma:
Producidos artificialmente:
En las pantallas planas.
Materia expulsada para la propulsión de cohetes.
Las descargas eléctricas de uso industrial.
Las bolas de plasma.
La gelatina
Plasmas terrestres:
Los rayos durante una tormenta.
La ionosfera.
La aurora boreal.
Plasmas espaciales y astrofísicos:
Las estrellas
Los vientos solares.
El medio interplanetario y el medio intergaláctico
Las nebulosas intergalácticas.
Ambiplasma
Estado Coloide:
Es un sistema físico-químico compuesto por dos fases: una continua que es fluida y otra dispersa en forma de partículas; por lo general sólidas. El nombre coloide proviene del griego kolas que significa que puede pegarse. Esto nombre hace referencia a la propiedad que tienen los coloides a tender a formar coágulos de forma espontánea.